设为首页
设为首页 收藏本站
收藏本站导读:本文汇总了目前全国(不包括港澳台)31个省、直辖市、自治区及部分市级政府已颁布的支持生物医药产业创新、促进临床试验发展的最新政策措施中的主要内容和重点解析,以及截止到2021年12月30日全国各地已备案的药物临床试验机构和医疗器械临床试验机构总数。为方便大家阅读,将按中国行政区划分4部分进行介绍。
生物医药产业作为国家战略性新兴产业正快速由最具有发展潜力的高技术产业向高技术支柱产业发展。在中央的政策支持下,各省、市级政府亦陆续出台了大量的支持性政策,以推动各地区的生物医药产业发展升级。
《天津市生物医药产业发展“十四五”专项规划》提出:增强临床试验对生物医药产业发展的支撑能力。推动医疗机构开展临床试验,支持有资质的医疗机构设立研究型病房,探索以多种合作方式建立临床试验协同网络,引导有资质的医疗机构承担仿制药人体生物等效性或临床有效性试验研究工作。鼓励医务人员积极参与药物临床研究,临床研究和临床试验情况纳入考核重要参考。
河北省人民政府办公厅印发关于《支持医药产业发展若干措施》的通知:创新药及改良型新药按进入临床试验不同阶段给予数额不等的奖励。支持医疗器械产业化。获创新器械特别审查程序,择优列入省级科技计划的项目,给与专项经费支持;通过创新器械特别审查程序,新获三类医疗器械注册证且在省内落地的产业化项目,择优纳入省高技术产业化项目计划,给予省战略性新兴产业专项资金支持。
江苏省《关于促进全省生物医药产业高质量发展若干政策措施的通知》中指出:对已取得临床试验机构资质的医院,可用于临床研究的床位数量不少于30张,按照不低于30%的比例逐年递增,到2024年,临床研究床位数占医院编制床位总数比例提高至10%左右。
广东省《关于生物医药创新发展的若干政策措施》:支持医疗机构开展临床试验,将临床试验条件和能力评价纳入医院等级评审。支持建立临床研究型医院,对已取得临床试验机构资质的三甲医院按总床位一定比例设置临床研究床位,或独立设置临床研究院区;临床试验的病床不纳入医院床位考核指标,完善绩效分配激励机制,临床试验视同科研项目纳入科研绩效考评,临床试验研究人员职务及职称晋升享受同等待遇。
与此同时,围绕加强生物医药创新及临床研究人才队伍建设,优化审评监督机制,完善监管与监督服务,加大金融支持力度,强化政策协同推进落实等方面,各省、市、自治区政府文件均做出了明确的表述,制定了各种保障措施
以下是各地政府支持医药创新和临床试验主要政策措施大汇总与重点解析之第一部分:华北地区和东北地区
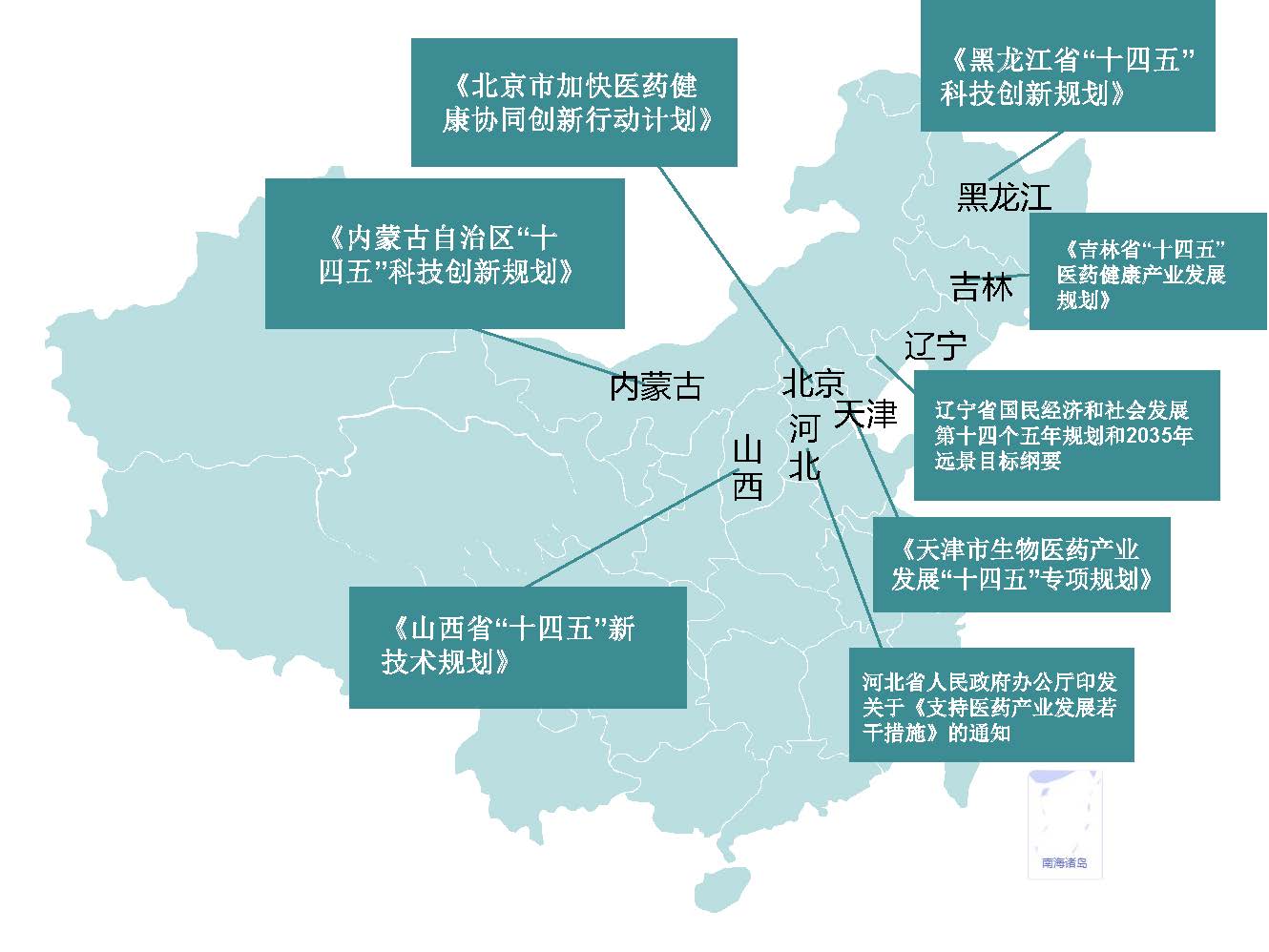
各地政府支持医药创新和临床试验主要政策措施汇总与重点解析一览表(华北、东北)
资料来源:各省、市、自治区政府官网